前沿进展
胃癌等实体瘤通过CXCL12-CXCR4轴招募大量多形核髓源性抑制细胞(PMN-MDSC),形成免疫抑制肿瘤微环境,使PD-1/PD-L1抗体抗体疗效受限。6月26日,Cancer Cell(IF 44.5)在线发表哥伦比亚大学与Tonix Pharmaceuticals合作的研究论文“A CXCR4 partial agonist improves immunotherapy by targeting immunosuppressive neutrophils and cancer-driven granulo-poiesis”,报道一种全新策略——CXCR4部分激动剂TFF2-MSA,能够精准调节CXCR4信号,选择性清除抑制性中性粒细胞,协同PD‑1抗体,在多种胃癌模型中显著抑制肿瘤、减少转移并延长生存期。
目前,哥伦比亚大学已将TFF2技术的治疗应用授权给Tonix Pharmaceuticals(NASDAQ:TNXP)。
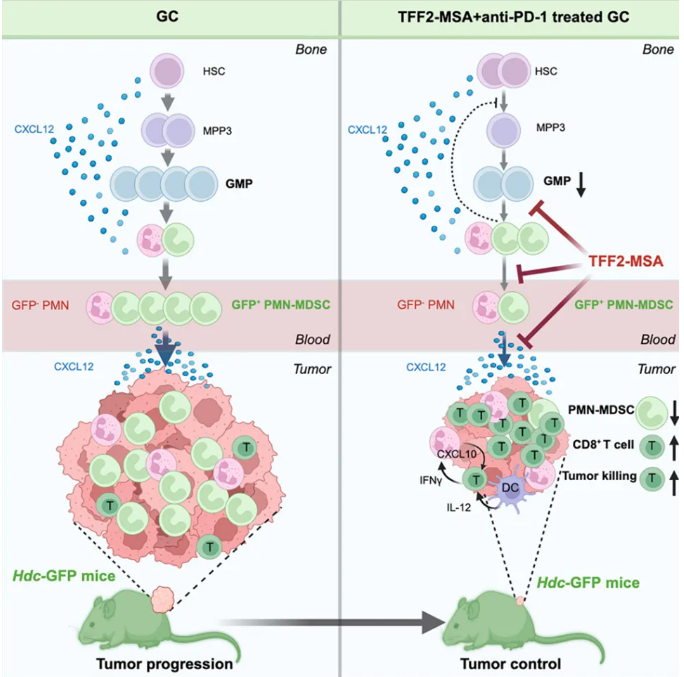
研究问题与核心发现
趋化因子受体CXCR4是调控粒细胞生成和PMN-MDSC招募的关键因子,既往尝试用CXCR4 完全拮抗剂阻断通路的效果不尽如人意,骨髓启动代偿性造血,未成熟粒细胞倾巢而出,反而加剧肿瘤进展。而且肿瘤中的中性粒细胞高度异质,有促癌的,也有抗癌的,是否可以精准去“坏”留“好”?
Trefoil Factor 2(TFF2)是分泌型的CXCR4部分激动剂,能够削弱完全激动剂CXCL12引起的过度激活,又能维持一定程度的CXCR4激活。
为了更有效地靶向PMN-MDSC,作者将TFF2与小鼠血清白蛋白(MSA)融合,构建了更稳定的TFF2-MSA,在一系列胃癌模型中评估了TFF2-MSA与PD-1抗体联合治疗的效果,随后通过多种方法全面探索其作用机制,并在病人样本中评估临床相关性。
文章核心发现包括:
-
TFF2-MSA在胃癌模型中协同增效PD-1单抗;
-
TFF2-MSA选择性减少免疫抑制性中性粒细胞和癌症驱动的粒细胞生成;
-
联合疗法显著诱导CD8+ T细胞抗肿瘤;
-
胃癌患者血浆TFF2降低,并与PMN-MDSC升高关联。
Tonix官方解读
Tonix公司于7月2日发布新闻,CEO Seth Lederman博士介绍,“在动物模型中,mTFF2-MSA与PD-1抗体的联合疗法展示了逆转PD-1抗体耐药的巨大前景。我们相信,已发表的数据支持进一步开发TNX-1700,使其成为克服胃癌和其他肿瘤对PD-1免疫疗法耐药性的一种方法。”
小鼠TFF2-MSA是Tonix在研管线TNX-1700的小鼠版本,TNX-1700是人TFF2和人血清白蛋白的融合蛋白,目前处于治疗胃癌和结直肠癌的临床前研究阶段。
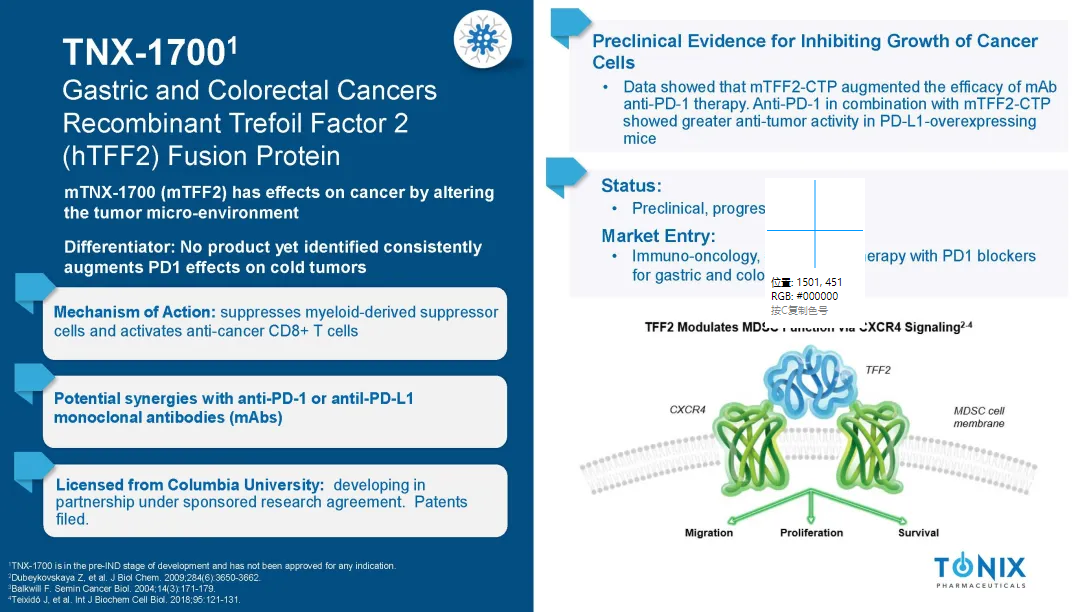
2025年7月7日Tonix Investor Presentation中有关TNX-1700的介绍
Bio X Cell体内抗体助力
这项研究大量地使用小鼠模型,其中仅正文图1就用了近250只模型小鼠,如果加上图1相关的补充图1-3,仅仅是评估联合疗法的疗效就惊人地使用了将近400只模型小鼠!而来自Bio X Cell的12种高品质体内功能级抗体,被用于从疗效评估到机制研究的多个环节,为这项研究成果做出了重要贡献。如需购买Bio X Cell产品,咨询产品技术问题,请联系Bio X Cell授权代理商欣博盛生物。
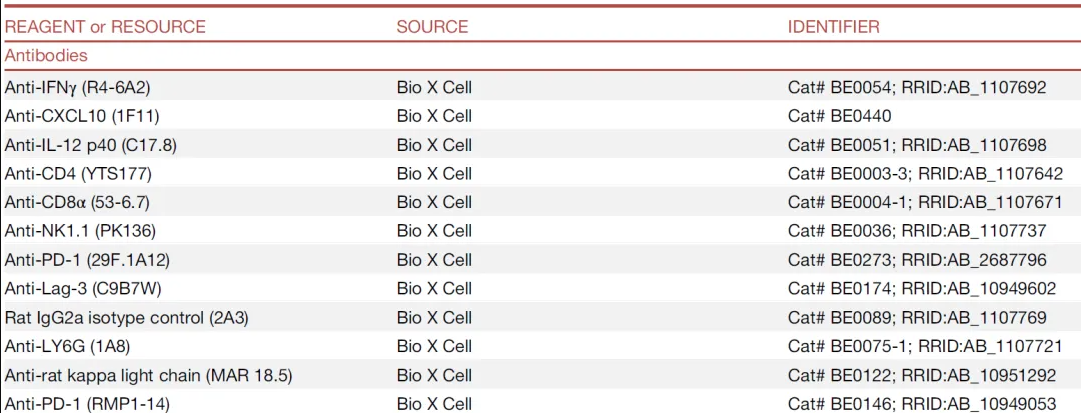
Key resources table部分截图
01稳健基线治疗评估联合疗法疗效
既然研究的是如何解除耐受,增强免疫检查点抑制剂(ICB)疗效,当然离不开Bio X Cell当家花旦PD-1抗体,#BE0273(克隆29F.1A12)和#BE0146(克隆RMP1-14)齐上阵,并与TFF2-MSA形成强效协同。LAG-3抗体(克隆C9B7W)也来助攻,证明TFF2-MSA对ICB具有广泛的增强潜力。
文章中用于比较单药与联合疗法疗效的小鼠模型包括:
-
代表混合型胃癌的ACKP(Atp4b-Cre;Cdh1−/−;LSL-KrasG12D/+;Trp53−/−)细胞构建的皮下移植瘤、原位移植瘤、门静脉肝转移以及手术切除后的自发性肺转移模型,并在皮下模型中加入化疗作为一线治疗;
-
代表肠型胃癌的PC(Trp53-/-;CCNE1-overexpressed)类器官移植瘤;
-
代表原发弥漫性胃癌的诱导RHOAY42C/Y42C突变加Cdh1缺失(Mist1-CreERT;Cdh1flox/flox;LSL-RHOAY42C/Y42C;Hdc-GFP)小鼠模型;
-
其他胃肠道癌症模型,包括CT26结肠癌皮下、原位模型以及Panc02胰腺癌模型;
-
ACKP皮下模型中TFF2-MSA联合LAG-3抗体治疗,评估TFF2-MSA的普适性。
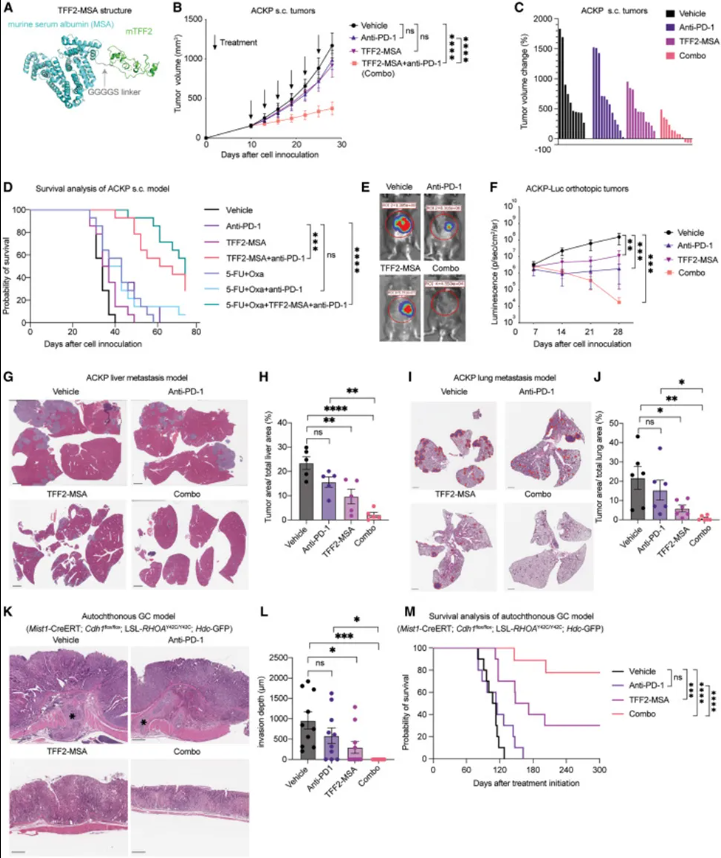
原文图1,TFF2-MSA与PD-1单抗协同抑制肿瘤生长和转移,并延长小鼠生存期
体内抗体具体使用方法:
待肿瘤长到合适大小后,PD-1抗体每三天腹腔注射10mg/kg,LAG-3抗体每只小鼠每三天腹腔注射200μg,对照组(vehicle)注射#BE0089(克隆2A3,10mg/kg)同型对照。
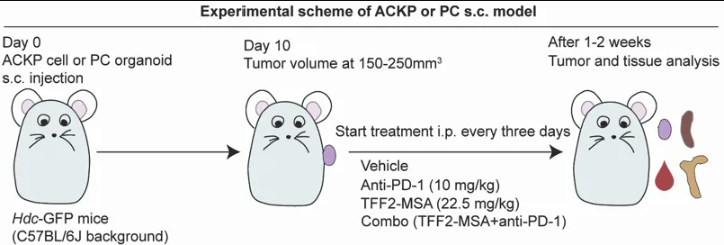
由ACKP细胞或PC类器官建立皮下瘤模型并接受治疗的实验方案
02体内细胞清除锁定抗肿瘤关键亚群
流式分析及scRNA-seq结果显示TFF2-MSA及联合疗法增加了肿瘤内的CD8⁺ T细胞,尤其是细胞毒性CD8+ T细胞以及IFNγ+TNFα+多功能CD8⁺ T细胞。
进一步使用Bio X Cell抗体#BE0003-3(CD4抗体,克隆YTS177)、#BE0004-1(CD8α抗体,克隆53-6.7)和#BE0036(NK1.1抗体,克隆PK136)在小鼠体内清除淋巴细胞,结果只有清除CD8+细胞能够完全消除联合疗法对肿瘤的抑制作用,说明CD8+ T细胞是TFF2-MSA协同增强PD-1的关键细胞类型。
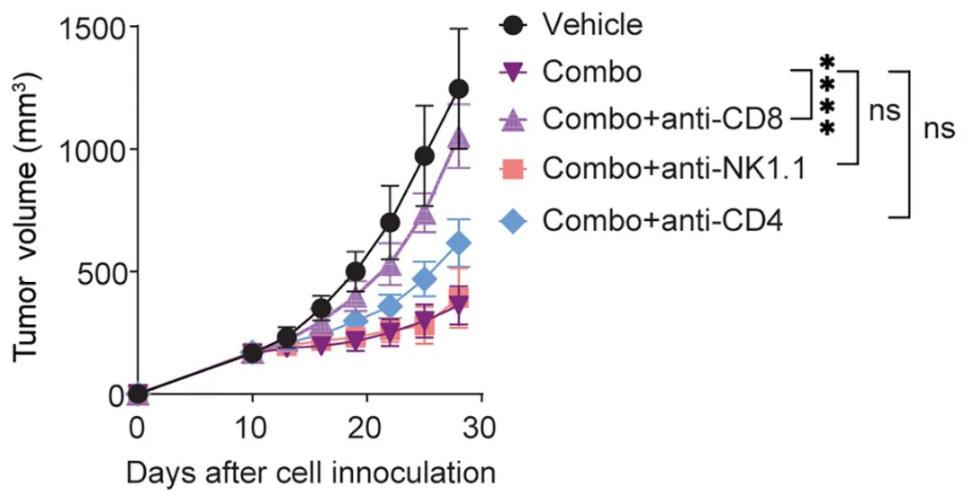
小鼠体内清除CD8+ T细胞完全消除联合疗法对肿瘤的抑制作用
体内抗体具体使用方法:
从TFF2-MSA和PD-1抗体开始治疗前一天开始,每三天腹腔注射CD4抗体20mg/kg,CD8α抗体20mg/kg或NK1.1抗体30mg/kg,对照组使用#BE0089(克隆2A3)同型对照。
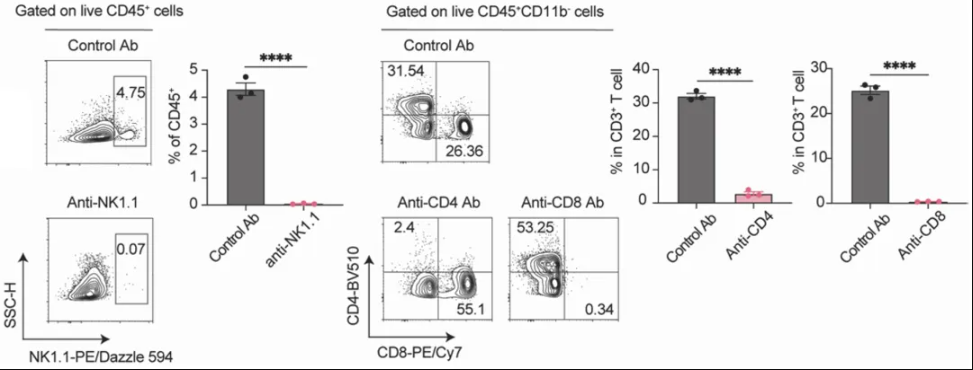
流式分析验证体内淋巴细胞清除效果
03细胞因子中和揭示免疫协同互作
scRNA-seq还发现高表达IL12b的树突状细胞在联合疗法治疗后占比升高,作者推测IL12+ DC、IFNγ+ CD8+ T细胞与治疗后保留的免疫刺激型PMN之间存在协同互作。
应用Bio X Cell抗体#BE0054(IFNγ抗体,克隆R4-6A2)、#BE0051(IL-12 p40抗体,克隆C17.8)和#BE0440(CXCL10抗体,克隆1F11)在小鼠体内中和IFNγ、IL-12或是Hdc-GFP- PMN表达的CXCL10,确实逆转ACKP肿瘤对联合疗法的响应,表明该疗法能激活先天免疫和适应性免疫,放大CD8+ T细胞的抗肿瘤效应。
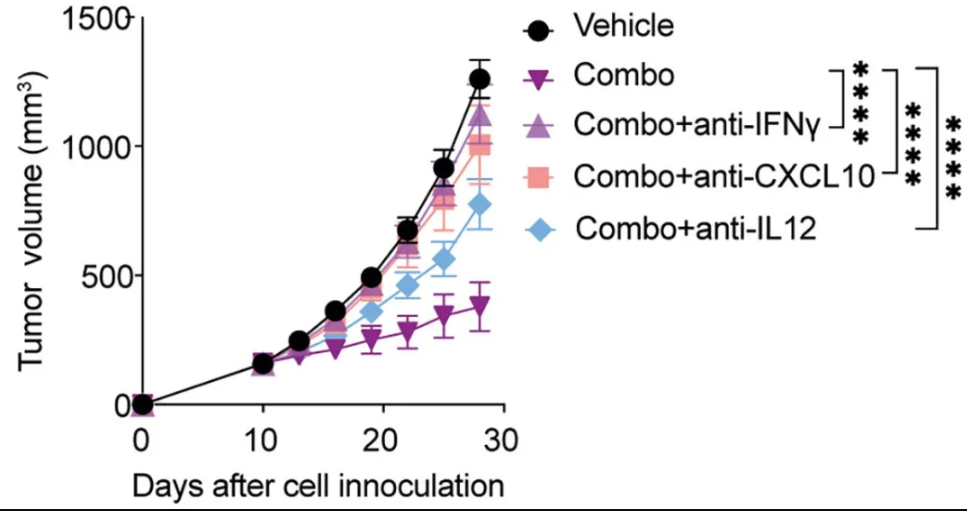
小鼠体内中和IFNγ、IL-12或CXCL10逆转肿瘤对联合疗法的响应
体内抗体具体使用方法:
从TFF2-MSA和PD-1抗体开始治疗前一天开始,每三天腹腔注射IFNγ抗体10mg/kg,CXCL10抗体10mg/kg或IL-12抗体10mg/kg,对照组使用#BE0089(克隆2A3)同型对照。
04其他PMN靶向策略有效性比较
文章还比较了TFF2-MSA与现有的PMN靶向策略,比如PD-1单抗联合LY6G抗体(Bio X Cell #BE0075-1,克隆1A8)的有效性。
尽管采用了优化的使用方案,改善了对外周PMN的清除,LY6G抗体并未能显著增强ACKP肿瘤对PD-1单抗的响应,再次验证外周PMN清除往往引发PMN的代偿性生成。
有趣的是,在TFF2-MSA与PD-1单抗联合疗法的基础上,加入LY6G抗体反而降低联合疗法的疗效,表明联合疗法的疗效部分依赖于外周PMN,与上述CXCL10+ PMN的抗肿瘤结果一致。
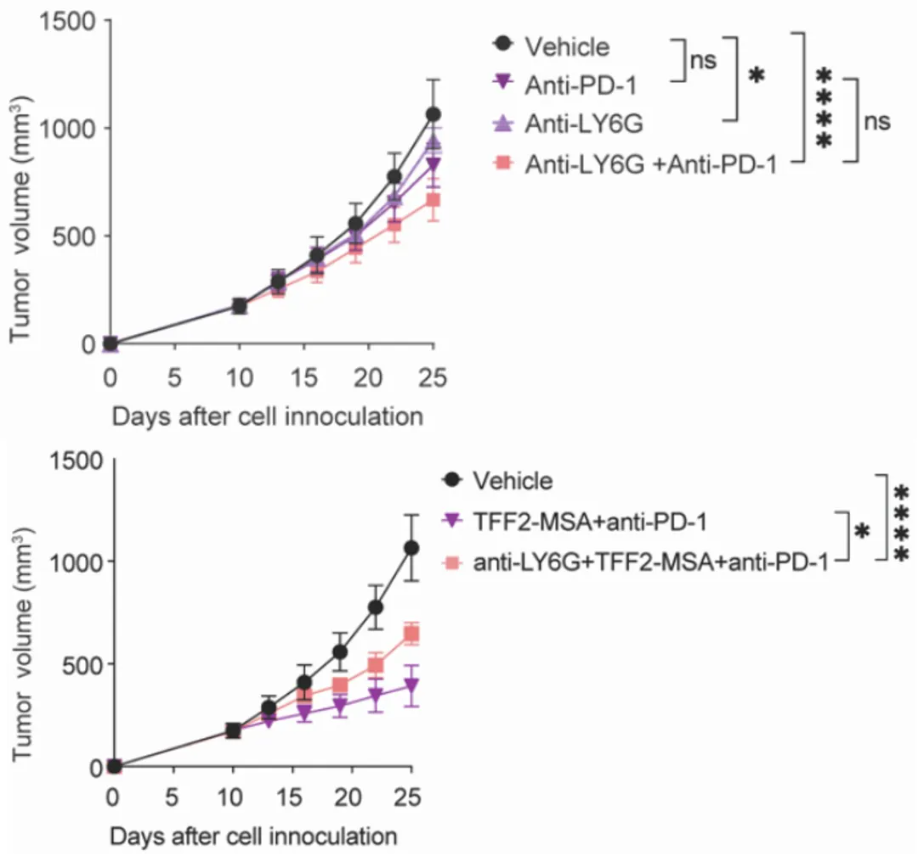
TFF2-MSA与LY6G抗体在小鼠体内清除总中性粒细胞的有效性比较
体内抗体具体使用方法:
作者采用了一种新近验证的改良方案来清除总中性粒细胞,从肿瘤细胞接种后7天开始,每只小鼠每隔一天注射200μg的LY6G抗体以及50μg的kappa轻链抗体(Bio X Cell #BE0122,克隆 MAR 18.5)。对照组为#BE0089(克隆2A3)同型对照。
从阻断免疫检查点到清除关键淋巴细胞,再到中和细胞因子、趋化因子,以及默默无闻始终相伴的同型对照,12支Bio X Cell InVivoMAb体内功能级抗体以高纯度、低内毒素、无叠氮的卓越品质,确保长达数周的体内应用既安全又高度可重复。
TFF2‑MSA在胃癌模型中证明了“半糖”调控的可行性,为突破PD‑1耐药提供新思路。Tonix TNX‑1700正加速迈向临床,而Bio X Cell的功能级抗体,将持续助力肿瘤免疫研究。
参考文献
1. Qian, J, et al (2025) A CXCR4 partial agonist improves immunotherapy by targeting immunosuppressive neutrophils and cancer-driven granulopoiesis. Cancer Cell. Online ahead of print. doi: 10.1016/j.ccell.2025.06.006.
2. Press release. Tonix Pharmaceuticals Announces Peer-Reviewed Publication in Cancer Cell Journal Highlighting Positive Preclinical Data of mTNX-1700 in Gastric Cancer Animal Models.
3. Tonix Investor Presentation - July 2025.

Bio X Cell,赋能每一次科学探索。

更多产品详情,请联系Bio X Cell授权代理商欣博盛生物
全国服务热线: 4006-800-892 邮箱: market@neobioscience.com
深圳: 0755-26755892 北京: 010-88594029
上海: 021-34613729 广州: 020-87615159
欣博盛代理品牌官网:www.nbs-bio.com
欣博盛品牌官网:www.neobioscience.net
